C’est la transformation progressive de la muqueuse de l’œsophage par de la muqueuse gastrique. C’est une lésion bénigne dont le risque principal est l’évolution vers le cancer. L’endobrachyoesophage ou oesophage de Barett (EBO) résulte de l’agression répétée de la muqueuse du bas œsophage par du liquide gastrique acide ou biliaire.
On estime que 10% de la population française a un reflux gastro-oesophagien et que 10% d’entre eux vont développer un EBO.
La transformation de l'endobrachyoesophage ou oesophage de Barett en cancer se fait par étapes successives :
Métaplasie intestinale → dysplasie de bas grade → dysplasie de haut grade → cancer
L’incidence du cancer chez les patients ayant un EBO asymptomatique est de 1 à 6 cas déclaré pour 1000 patients ayant un endobrachyoesophage ou oesophage de Barett par an.
Le diagnostic est endoscopique.
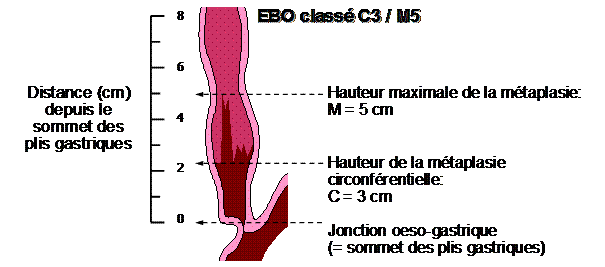
L’EBO peut être circulaire ou sous forme de languette. Il se mesure par la distance en cm entre la jonction oeso-gastrique et le haut de la métaplasie intestinale (classification de Prague).
Des biopsies en quadrant, 2-4 biopsies tous les 1 cm doivent être effectuées :
La surveillance de l’endobrachyoesophage ou oesophage de Barett dépend des résultats histologiques.
Les critères du traitement
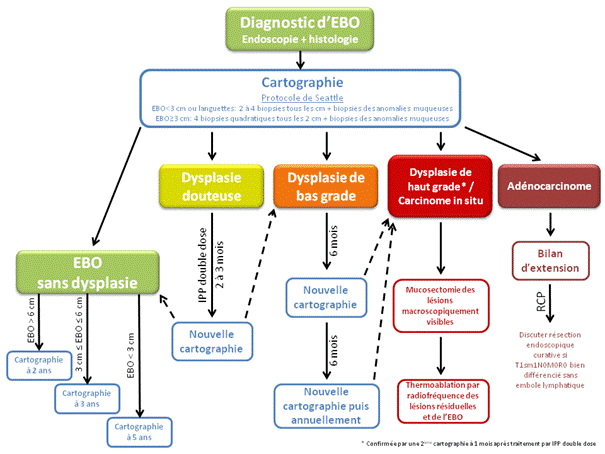
Dans le cas d’un EBO non dysplasique, les objectifs thérapeutiques sont la disparition des symptômes et des complications inflammatoires (ulcère, œsophagite et sténose peptique) du RGO et la prévention de l’apparition de la dysplasie voire du cancer.
Les inhibiteurs de la pompe à protons (IPP) garantissent dans la majorité des cas le contrôle de la symptomatologie douloureuse et la prévention des complications liées au reflux. Par contre, il n’existe à ce jour aucune preuve formelle de leur efficacité en termes de prévention de l’adénocarcinome œsophagien ou la chirurgie anti-reflux.
La SFED propose un rythme de surveillance différent en fonction de la hauteur de l’EBO :
- Pour un EBO de moins de 3 cm de hauteur: fibroscopie entre 3-5 ans
- Pour un EBO ayant une hauteur comprise entre 3 et 6 cm : fibroscopie à 2 ans
- Pour un EBO de plus de 6 cm de hauteur : fibroscopie à 2 ans.
L’identification d’une DBG sur un EBO doit être confirmée par une nouvelle série de biopsies, car le diagnostic histologique de DBG est difficile. Les recommandations de la SFED sont de refaire une nouvelle cartographie à 2-3 mois au décours d’un traitement par IPP double dose pendant cette période, les IPP limitant le risque de faux positif du à des lésions inflammatoires.
En cas de dysplasie de bas grade certaine, il n’y a actuellement pas de recommandation de traitement de cette dysplasie. Une simple surveillance rapprochée est proposée.
Cependant, compte-tenu de l’augmentation du risque d’évolution vers la dysplasie de haut grade et/ou l’adénocarcinome, et surtout de la grande efficacité de nouvelles méthodes endoscopiques pour éradiquer un EBO en DBG, comme la radiofréquence (RF) ou la mucosectomie endoscopique, beaucoup d’équipe préconise le traitement endoscopique de ces lésions ce qui est notre cas.
En cas de dysplasie de haut grade (DHG), ou de carcinome in situ, tout comme la dysplasie de bas grade, la SFED recommande une deuxième fibroscopie 1 à 2 mois après un traitement par IPP à double dose. Une double lecture anatomo-pathologique sera réalisée si possible. La DHG et le carcinome in situ sont des lésions limitées à la muqueuse sans risque d’envahissement ganglionnaire ou métastatique. Avant l’avènement des traitements endoscopiques, l’oesophagectomie était le traitement standard pour la prise en charge de telles lésions malgré une morbidité de 30 à 40% et une mortalité per et post-opératoire de 1 à 4%.
L’endoscopie a donc aujourd’hui, de fait, une place de premier choix dans la stratégie thérapeutique. Une écho-endoscopie doit être réalisée afin d’éliminer une infiltration tissulaire profonde ou un envahissement ganglionnaire.
En cas de découverte de ganglion suspect, une ponction sous écho-endoscopie devra être réalisée. En effet, il est important de réserver les indications des traitements endoscopiques éventuels aux lésions classées usT1N0.
Les techniques endoscopiques pour le diagnostic des zones suspectes
- La chromoendoscopie optique ou virtuelle augmente de plus de 30% la détection des zones dysplasiques.
La chromo endoscopie optique repose sur la vaporisation durant l’examen d’un produit qui va accentuer le relief de la muqueuse. Le plus souvent c’est l’acide acétique à 1,5% qui est utilisé. Il donne un aspect blanchâtre à la muqueuse et rehausse l’architecture glandulaire.
- La chromoendoscopie virtuelle
Elle est présente sur tous les endoscopes de haute définition. Il s’agit du NBI ou FICE qui rehausse les reliefs et permettent de zoomer.
- Une nouvelle technique : l’endomicroscopie confocale permet d’obtenir des images dynamiques internes en temps réel au cours d’une endoscopie. Le dispositif le plus utilisé est le Cellvizio. On introduit une mini sonde dans l’endoscope qui est au contact de la muqueuse et on injecte par voie IV un agent de contraste fluorescent. Le seuil de détection des lésions pré néoplasiques passe de 40 à 96%.
Traitement de l'endobrachyoesophage ou oesophage de Barett
Deux principaux groupes de techniques endoscopiques sont disponibles : les techniques de résection endoscopique (mucosectomie, dissection sous muqueuse) et les techniques de thermoablation (radiofréquence).
- La mucosectomie endoscopique : cette technique consiste en la résection de la muqueuse et d’une partie de la sous-muqueuse œsophagienne. La technique utilisée dans le service associe la mise en place d’un élastique après injection sous-muqueuse permettant dans un deuxième temps la résection de la lésion à l’anse.
- La dissection sous-muqueuse : c’est la technique la plus récente. Elle consiste à disséquer pas à pas la muqueuse et la sous-muqueuse de la musculeuse à l’aide de couteaux endoscopiques spécifiques. Les avantages de la DES par rapport à la mucosectomie œsophagienne sont de pouvoir mieux contrôler les plans de dissection et surtout d’obtenir une résection dite en bloc, afin de faciliter l’interprétation histologique et de limiter le risque de récidive. Cette technique plus récente qui nécessite un apprentissage est utilisée en cas d’EBO étendu.
- La radiofréquence : la radiofréquence a été introduite récemment pour traiter les EBO comportant de la dysplasie sévère et en cas de carcinome superficiel de l’œsophage. Elle peut être associée à la mucosectomie. La Radiofréquence utilise une onde de coagulation qui détruit les micro-vaisseaux et dénature les protéines cellulaires. La profondeur d’action de cette onde est calibrée, fixe et contrôlée, l’ensemble permettant la thermoablation de l’EBO et des lésions associées. La principale complication est le risque de sténose oesophagienne.
- La radiofréquence oesophagienne est une nouvelle technique endoscopique de destruction des tumeurs oesophagiennes superficielles et représente une alternative au traitement chirurgical. Cette technique permet de traiter l’EBO avec une dysplasie de haut grade Après plusieurs séances de radiofréquence, la réponse complète sur la dysplasie et sur la métaplasie intestinale est excellente, supérieure à 90 % dans la grande majorité des études publiées. En cas de dysplasie de bas grade, même s’il n’y a pas de recommandation actuelle, son intérêt est également démontré.
Les complications majeures sont exceptionnelles (perforation, hémorragie). Les sténoses sont rares. Les complications mineures (douleur rétrosternales) sont contrôlées par un traitement symptomatique
Le traitement par radiofréquence utilise un courant sinusoïdal de 400 à 500 MHz qui induit une coagulation des micro-vaisseaux et une dénaturation des protéines cellulaires. La radiofréquence entraîne une destruction homogène de la muqueuse et de la sous-muqueuse sur environ 1 mm de profondeur. Ce courant, délivre par un générateur, est transmis à la muqueuse par des électrodes bipolaires. Les résultats sont encourageants puisqu’on parle d’un taux de 85,7 % d’éradication de la dysplasie
Le parcours du patient
Le traitement par radiofréquence se fait en deux séances. Le patient est hospitalisé 2 jours pour bénéficier de la 1re séance. Il est hospitalisé à nouveau, entre deux mois et trois mois plus tard, pour la 2e séance. Il entre ensuite dans un parcours de soins avec surveillance à 3 mois, 6 mois, un an, et ensuite tous les deux ans.
Le service de gastroentérologie de l’hôpital de la Croix Saint Simon a commencé à traiter les patients qui présentent un endobrachyoesophage ou oesophage de Barett avec dysplasie de haut grade depuis janvier 2017.


